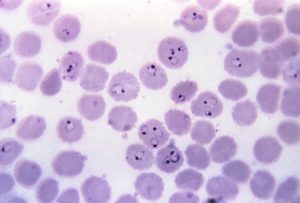
Un equipo de investigadores de la Estación Biológica de Doñana (EBD) en Sevilla y del Instituto de Parasitología y Biomedicina “López-Neyra” de Granada, centros del Consejo Superior de Investigaciones Científicas (CSIC), arroja nueva luz acerca de los mecanismos mediante los cuáles Plasmodium falciparum (causante de la malaria) regula la expresión de genes a lo largo de su ciclo de vida.
El peligro de la malaria
La malaria humana es responsable de más de medio millón de muertes al año, la mayoría niños y mujeres embarazadas; y el Plasmodium falciparum es la especie de parásito más prevalente en África y la más mortífera. Según la Biblioteca Nacional de Medicina de EE.UU.:
La malaria es causada por un parásito que se transmite a los humanos a través de la picadura de mosquitos Anofeles infectados. Después de la infección, los parásitos (llamados esporozoítos) viajan a través del torrente sanguíneo hasta el hígado, donde maduran y producen otra forma de parásitos, llamada merozoítos. Los parásitos ingresan en el torrente sanguíneo e infectan a los glóbulos rojos. Los parásitos se multiplican dentro de los glóbulos rojos, los cuales se rompen al cabo de 48 a 72 horas, infectando más glóbulos rojos. Los primeros síntomas se presentan por lo general de 10 días a 4 semanas después de la infección, aunque pueden aparecer incluso a los 8 días o hasta un año después de esta. Los síntomas ocurren en ciclos de 48 a 72 horas.
La malaria humana es una enfermedad devastadora. Más de medio millón de personas mueren al año, muchos de ellos niños en el África sub-sahariana, y su incidencia a nivel mundial es de entre de 200 y 300 millones de casos, según la Organización Mundial de la Salud (OMS), lo que significa alrededor del 40% de la población mundial. Por ello es también mayor causa de pobreza. Plasmodium falciparum es la especie de parásito mas prevalente en África y la responsable de más muertes a nivel mundial. Pese a los avances en materia de investigación, en la actualidad no existe vacuna efectiva contra la malaria.
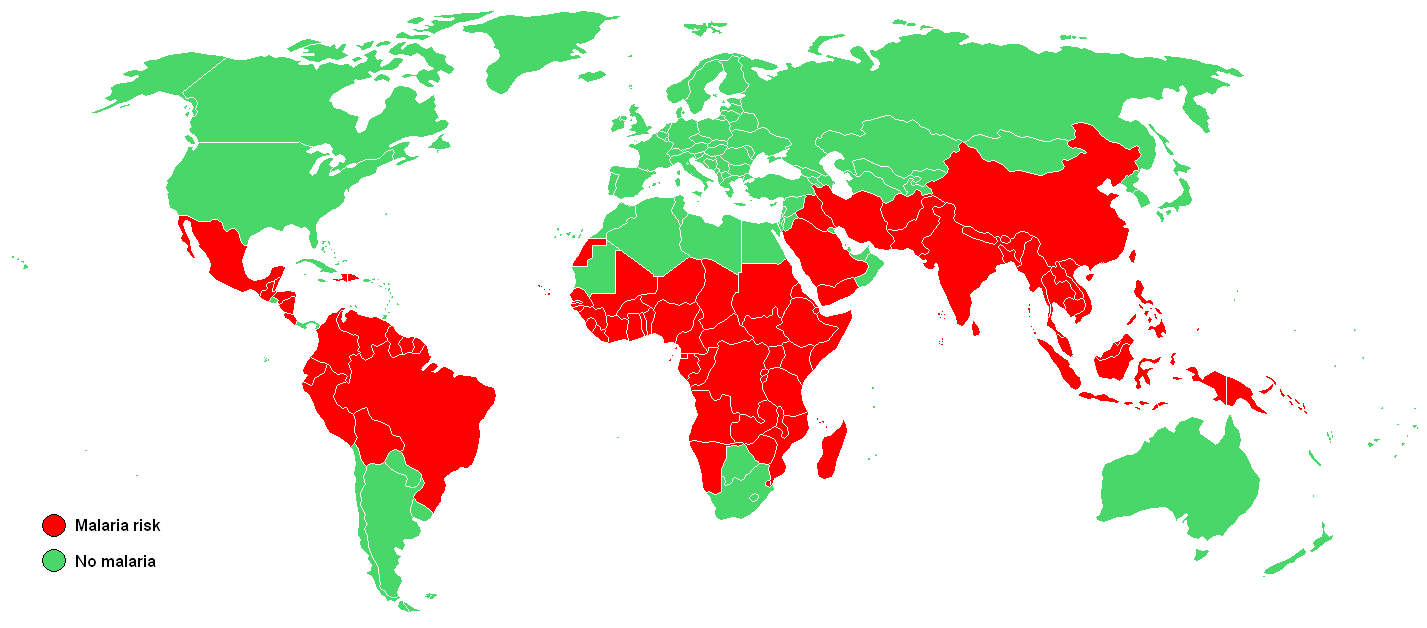
Mapa del riesgo de malaria
Una nueva técnica para estudiar la malaria
El estudio utiliza una técnica pionera, el ATAC-seq, para caracterizar el estado de accesibilidad de la cromatina en el parásito de la malaria y relacionarlo con los genes que se activan en las diferentes etapas de su ciclo de vida. La comparación de líneas de parásitos que difieren en su virulencia permite identificar los factores reguladores de genes clave para el desarrollo de la enfermedad. El estudio de las regiones abiertas del genoma de este parásito les ha permitido identificar las secuencias y los factores reguladores que encienden y apagan los genes, entre ellos genes implicados en la virulencia del parásito. La investigación aparece en el último número de Nucleic Acids Research y es el resultado de una colaboración con investigadores del Centro Andaluz de Biología del Desarrollo (CABD) de Sevilla y del Instituto de Salud Global de Barcelona.
El parásito de la malaria humana utiliza mecanismos de tipo epigénetico, cambios en la expresión de los genes sin cambios a nivel de la secuencia de ADN, para adaptarse a las condiciones del ambiente cambiante a lo largo de su ciclo de vida en el huésped humano y el mosquito. Pese a su importancia desde un punto de vista de salud global, aún se desconoce mucho acerca de los mecanismos que le permiten al parásito regular la función de los genes.
“El estudio de estas regiones permite también predecir las proteínas implicadas la activación de los genes. Se trata de uno de los primeros estudios en aplicar está metodología”, explica Elena Gómez-Díaz, responsable del estudio.
Los autores también han comparado los perfiles de accesibilidad en dos líneas celulares del parásito que difieren en su virulencia, y esto les ha permitido identificar los mecanismos de regulación subyacentes. Hay muchas ejemplos de genes de virulencia que varían su expresión de un parásito a otro, incluso siendo su genoma idéntico, y esto da lugar a una variante de la proteína distinta. Esta estrategia es clave para la adaptación del parásito: un cambio en la proteína permite al parásito de la malaria camuflarse y evadir el sistema inmunitario humano. Estudiando estas familias de genes de virulencia, los autores han determinado que la activación de un gen especifico, de los muchos posibles, está relacionada con la accesibilidad en su promotor, aunque también están implicados ARNs no codificantes.
El reto ahora es aplicar esta misma técnica a otras etapas del ciclo de vida del parásito que son clave para la transmisión, como son el ciclo de desarrollo en el mosquito, y en lo que están trabajando ahora, apunta la investigadora.
Bibliografía:
José Luis Ruiz, Juan J Tena, Cristina Bancells, Alfred Cortés, José Luis Gómez-Skarmeta, Elena Gómez-Díaz; Characterization of the accessible genome in the human malaria parasite Plasmodium falciparum, Nucleic Acids Research, , gky643, https://doi.org/10.1093/nar/gky643