 Dentro de los miles de genes que componen el genoma humano, la mayoría están repartidos en veintidós de los veintitrés pares de cromosomas en los que se reparte nuestro material genético. Cada uno de los miembros de cada pareja de cromosomas procede de uno de los progenitores, de manera que podríamos decir que todos los humanos tenemos dos copias o versiones de genoma, cada una de las cuales es una mezcla de las dos copias que tenían cada uno de los padres, y así sucesivamente hacia atrás en nuestro árbol genealógico. Sin embargo, hay unos cuantos genes que van en vehículos un poco más especiales. Entre ellos, están los genes que viajan en el último par de cromosomas que conforman nuestro genoma: el par 23 o par sexual, que presenta la particularidad de que juega con dos cromosomas distintos en lugar de con copias de un mismo cromosoma.
Dentro de los miles de genes que componen el genoma humano, la mayoría están repartidos en veintidós de los veintitrés pares de cromosomas en los que se reparte nuestro material genético. Cada uno de los miembros de cada pareja de cromosomas procede de uno de los progenitores, de manera que podríamos decir que todos los humanos tenemos dos copias o versiones de genoma, cada una de las cuales es una mezcla de las dos copias que tenían cada uno de los padres, y así sucesivamente hacia atrás en nuestro árbol genealógico. Sin embargo, hay unos cuantos genes que van en vehículos un poco más especiales. Entre ellos, están los genes que viajan en el último par de cromosomas que conforman nuestro genoma: el par 23 o par sexual, que presenta la particularidad de que juega con dos cromosomas distintos en lugar de con copias de un mismo cromosoma.
Se trata de los cromosomas X e Y, descritos por primera vez por la investigadora inglesa Nettie Stevens (1861-1912), en un contexto en el que todavía no se tenía demasiado claro cuál era la función de los cromosomas ni qué relación tenían con los genes. Todavía no se había descubierto la estructura del ADN (ni siquiera habían nacido Rosalind Franklin y haría falta llegar a 1944 para que Avery, McCleod y McCarty demostraran que el ADN era el sustrato que componía los cromosomas y que, a su vez, era el que portaba la información genética). Stevens confirmó, no obstante, que, en los seres humanos, la composición cromosómica de los hombres es distinta a la de las hembras en este par: las células de las hembras tienen dos cromosomas X, pero en las células de los machos el segundo cromosoma X está sustituido por un cromosoma Y. Por tanto, son los espermatozoides los que determinan si el cigoto resultante va a corresponder a una hembra (si portan un cromosoma X) o a un macho (si portan un cromosoma Y), claro que ahora sabemos que esto no es siempre así. Ya le dedicamos un artículo ex profeso a la determinación del sexo en los seres humanos, pero, ¿todos los genes de los cromosomas sexuales tienen que ver, de hecho, con el sexo? ¿Qué pasa con esos genes? ¿Se heredan distintos en chicos y chicas? ¿Qué hacen las chicas con dos cromosomas X y los chicos solamente con uno? ¿Hay diferencias en la expresión? Y, si no las hay, ¿cómo es eso posible?
Mosaico de equises
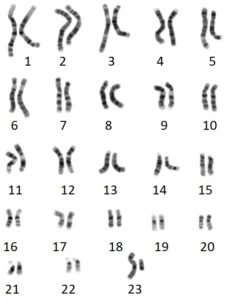
Cariotipo humano donde se indican las veintitrés parejas de cromosomas
Lo primero que quizás habría que matizar es que los cromosomas sexuales no se llaman así porque contengan todos los genes necesarios para constituir el sexo de un individuo (ni mucho menos); sólo se llaman así porque guardan las llaves primeras que abren o cierran una vía u otra de desarrollo sexual activando a otros genes. El cromosoma X, sin ir más lejos, guarda muchos genes relacionados con cosas que no tienen nada que ver con el sexo pero cuya herencia se ve reflejada en él. Por esta razón, decimos que son genes ligados al sexo. Los más conocidos son los genes para la visión en color (cuyo defecto produce el típico daltonismo o ceguera para el rojo y el verde) o para varios factores de coagulación (cuya ausencia produce distintos tipos de hemofilia, según el que falte). Por mera naturaleza del ADN, existen cromosomas X en la población que tienen alguno de estos genes estropeados, que no funcionan, no producen proteínas funcionales. Cuando coinciden en un cigoto dos cromosomas alterados en el mismo gen, entonces la hembra resultante tendrá la enfermedad correspondiente. Sin embargo, si coinciden un cromosoma con el gen funcional y otro defectuoso, entonces, en principio, no importa que haya una versión del gen estropeada: con una nos basta para ir tirando. Por eso se dice que las enfermedades como el daltonismo o la hemofilia son recesivas en mujeres, ya que sólo se manifiestan en condición de homocigosis, cuando coinciden dos cromosomas igual de tocados. En heterocigosis, la mujer es portadora. No se nota que tiene la copia estropeada, en el caso de las enfermedades que se producen por genes que no funcionan. En los hombres, en cambio, como sólo tienen un cromosoma X, lo que éste tenga asignado va a misa, ya que no hay otro cromosoma con el que compensar la carencia.
Sin embargo, no hemos tocado un punto importante. Y es que no tiene ningún sentido, a priori, que unos individuos tengan una ración de cromosoma y otros individuos tengan doble ración. ¿Cómo se regula eso? ¿Qué sucede si los dos cromosomas X fueran funcionales pero tuvieran dos genes expresándose dando proteínas distintas? ¿Las mujeres expresan más proteínas que los hombres? ¿O son los hombres los que duplican la expresión de su único cromosoma X para que al final todos los humanos tengamos el mismo grado de expresión génica? ¿Acaso es esto importante?
Pues lo cierto es que si miramos a otros organismos, la cosa podría cambiar un poco nuestra versión de los hechos. Por ejemplo, en la mosca de la fruta, que tiene un sistema también basado en cromosomas X e Y, el macho duplica la expresión de su cromosoma X, de forma que aunque sólo tiene uno, al final tiene la misma cantidad de productos génicos que las hembras. Cabe anotar que la determinación sexual de esta mosca es un poco diferente al de los humanos, porque aquí no es el cromosoma Y el que determina el ser macho, sino que es por la proporción entre cantidad de cromosomas X y cromosomas no sexuales, pero para el caso no nos importa esta diferencia. En los seres humanos, sin embargo, la cosa va al revés: en todas las células de la hembra, uno de los cromosomas X es inactivado, al azar, formando un grumo de ADN silenciado para siempre que llamamos corpúsculo de Barr. De esta manera, solamente uno de los cromosomas X de cada célula está funcional tanto en hombres como en mujeres, fenómeno que conocemos como “compensación de dosis”. Puede parecer una tontería, pero ponemos atención en que el que haya un cromosoma de más o de menos en las células de un ser humano altera, a veces de forma muy profunda, el desarrollo de los individuos. La más famosa es la trisomía del cromosoma 21, que conduce al síndrome de Down, pero hay casos mucho más fuertes y graves, como el síndrome de Patau (trisomía en el cromosoma 13), que causa una constelación de malformaciones fetales de la que no se espera que los bebés sobrevivan más de tres meses tras su nacimiento. Es decir: importa, y mucho, el que los cromosomas estén en su número y se expresen a un nivel que el organismo demande.
Sin embargo, hemos dicho que las mujeres, por tener doble ración de cromosoma X, pueden ser heterocigotas y no sufrir enfermedades como el daltonismo o la hemofilia. ¿Cómo se come esto si estamos diciendo al mismo tiempo que uno de los cromosomas se inactiva? ¿Qué sucede si se inactiva el cromosoma sano y se queda encendido el enfermo? ¿Puede una mujer heterocigota para la hemofilia ser hemofílica por culpa de la compensación de dosis? Pues lo cierto es que, con toda seguridad, las mujeres heterocigotas para alguna de estas enfermedades (y tantas otras que no hemos citado) tienen su cromosoma sano inactivado, pero sólo en algunas (más o menos, la mitad) de todas sus células. En realidad, la inactivación del X ocurre de forma azarosa y, sobre todo, independiente en cada una de las células. La retina de una mujer heterocigota para el daltonismo tiene células que, efectivamente, son incapaces de ver el rojo y el verde, pero otras que sí lo son, y estas son suficientes para permitirle ver en color.

El caso es que en las mujeres humanas no se ve a simple vista un patrón de colores corporal que nos indique que son mosaicos genéticos, porque además la inactivación ocurre de forma distinta a en el caso de los gatos (no hay regiones enteras a trozos grandes). Lo más sorprendente es que no sólo es un hecho poco conocido en ciencia, sino poco investigado a nivel de implicaciones médicas. Se sabe muy poco (o nada, en muchos casos) sobre cómo el cuerpo de la mujer heterocigota lidia con unas células con unos cromosomas X y con sus contrarias conviviendo. Hay 1.100 genes del cromosoma X, la mayoría de los cuales son exclusivos de él, que influyen en muchos genes del genoma: no es una cuestión en absoluto banal, especialmente teniendo en cuenta las implicaciones que eso podría tener a efectos de ciertos fármacos, por ejemplo.
A tortas con el Y
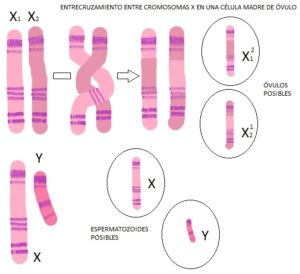
Recombinación del cromosoma X frente a la imposibilidad de recombinación del cromosoma Y. Mientras que el hombre produce miles de millones de espermatozoides al día, de los cuales menos del 5% -con suerte- son viables, la mujer tiene en sus ovarios, en el momento en el que nace, todos los óvulos que va a liberar a lo largo de su vida
El cromosoma Y tiene el dudoso honor de estar solo en el genoma. Solo tiene una pequeña porción de su anatomía que coincide con el cromosoma X lo suficiente como para poder emparejarse con él durante la división celular y repartirse correctamente entre las células hijas. Por lo demás, no tiene posibilidad alguna de recombinación con otros cromosomas. Como es sabido, la recombinación es un mecanismo muy importante por el cual los cromosomas de cada pareja intercambian pedacitos homólogos el uno del otro, intercambiándose versiones génicas. Es algo que sucede de forma rutinaria en las células que forman los espermatozoides y los óvulos y que viene a significar que el cromosoma 2 que heredaste de tu madre, digamos, es una mezcla de los dos cromosomas 2 que tenía la susodicha, que a su vez es son sendos remixes de los cuatro cromosomas 2 que tenían tus abuelos maternos. Sin embargo, ¿con quién se recombina el cromosoma Y? No hay células con dos cromosomas Y a la vez.
Hace unos 180 millones de años, este cromosoma no existía: era exactamente otro cromosoma X y el sexo se determinaba de otra manera. Sin embargo, hubo de aparecer un gen que adquiriese evolutivamente un papel clave en la determinación del sexo y entonces la recombinación entre el cromosoma X y el proto-Y fuera realmente un despropósito porque se mezclarían los genes sexuales primordiales. Así, la selección natural habría ido favoreciendo que el cromosoma X y el proto-Y fueran poco a poco diferenciándose, lo que hizo que dejaran de ser recombinables entre sí. Esto tuvo un efecto claramente positivo, ya que se extendió por los mamíferos en general hasta nosotros, pero claro: si un cromosoma Y acumula una mutación negativa, y otra, y otra, ¿cómo se libra de ellas? ¿Qué pasa si aparece una mutación muy buena y se junta en el mismo cromosoma con una mutación pésima? ¿Están los cromosomas Y malditos y condenados a desaparecer finalmente a causa de la acumulación irreversible de mutaciones con el paso de los siglos?
Esto es lo que en genética de poblaciones se conoce como Trinquete de Müller o lastre genético y es bastante palpable cuando vemos que los cromosomas Y apenas tiene genes funcionales. Sin embargo, cuando se compararon cromosomas Y de muchas especies de mamífero, se ha visto que la práctica totalidad de ellos tiene una proporción de genes similar, fundamentales para el desarrollo embrionario (no sólo para la determinación del sexo y también presentes en los cromosomas X de las hembras). Esto implica que el trinquete de Müller actuó conforme los cromosomas Y se separaron genéticamente de los X, pero la selección natural ha impedido que se propaguen cromosomas Y defectuosos en los genes esenciales, matando a todos los individuos cuyos Y mostraban alguna mutación y favoreciendo, pues, que estos pocos genes que el cromosoma Y porta se mantengan inalterados por el paso de las generaciones. Las enfermedades ligadas la Y son tremendamente raras debido a esto y, si sobreviven, la mayoría de hombres con algún defecto en el cromosoma Y son estériles, por lo que no pueden pasar el defecto a sus hijos. ¡Que no es lista la naturaleza ni ná!

Lejos de ser una licencia poética, los humanos -y, sobre todo, las mujeres- no somos monolitos celulares, sino que a nivel citogenético presentamos mosaicismo, microquimerismos, patrones de expresión distintos, etc. (Detalle del mosaico de la emperatriz bizantina Teodora y su séquito)
De todas formas, no es tan cierto ni tan sencillo que el cromosoma Y esté exclusivamente en los hombres. Y no lo decimos solamente por los casos de intersexualidad, donde se encuentran personas fenotípicamente mujeres a pesar de ser cariotípicamente hombres u hombres con doble ración de cromosoma X, sino porque cada vez sabemos más frecuente la existencia de microquimerismos en la mujer. Sin meternos mucho en materia, ya que el tema merece ser tratado aparte, se han encontrado células XY en mujeres XX. En 2012, sin ir más lejos, un estudio realizado en el Centro de investigación Fred Huchinson (Seatle) reportó casos de células XY en cerebros de mujeres fallecidas. Este mismo instituto, ya en 2004, encontró restos de ADN propiamente masculino en ciento veinte mujeres. En algunos casos, se propuso que los fetos masculinos intercambian algunas células con las de la madre y puede llegar a existir cierta población de células XY en el cuerpo femenino (sin saber si son meras expectadoras o tienen alguna repercusión). Sin embargo, el 8% de los casos no habían tenido nunca descendencia femenina y el 10% nunca habían tenido descendencia (aunque los autores proponen que tal vez haya existido algún tipo de aborto o la reabsorción de algún “hermano” mellizo). El caso, un auténtico enigma.
Hay muchas cosas, en conclusión, que no entendemos completamente sobre nuestros propios cuerpos ni nuestra propia genética. Que lo normal en nosotros es la heterogeneidad y que no es tan sencillo como nos lo cuentan los libros. Que aún nos queda mucho por investigar y por comprender y que, sin duda, estamos en un momento muy interesante de la Historia para estudiar y leer ciencia.
Fuentes y referencias bibliográficas
- MIGEON, B.R. (2007). Why females are mosaics, x-chromosome inactivation, and sex diffferences in disease. Gender Medicine, 4(2). pp: 97-105 | https://doi.org/10.1016/S1550-8579(07)80024-6
- BELLOTT, D. W.; HUGHES, J. F.; SKALETSKY, H.; BROWN, L. G.; PYNTIKOVA, T.; CHO, T., & amp. PAGE, D. C. (2014). Mammalian Y chromosomes retain widely expressed dosage-sensitive regulators. Nature. pp: 494-499 | https://doi.org/10.1038/nature13206
- CORTEZ, D.; MARIN, R.; TOLEDO-FLORES, D.; FROIDEVAUX, L.; LEICHTI, A.; WATERS, P. D.; GRÜTZNER, F.; KAESSMAN, H. (2014). Origins and functional evolution of Y chromosomes across mammals. Nature. 508: 488-493 | https://doi.org/10.1038/nature13151
- CHAN, W.F.; GURNOT, C.; MONTINE, T.J.; SONNEN, J.A.; GUTHRIE, K.A.; NELSON, J.L. (2012) Male microchimerism in the human female brain. PLOS ONE, 7(9): e45592. Bibcode:2012PLoSO…745592C. doi:10.1371/journal.pone.0045592. PMC3458919. PMID23049819.
- YAN, Z.; LAMBERT, N.C.; GUTHRIE, K.A.; PORTER, A.J.; LOUBIERE, L.S.; & amp. MADELEINE, M.M. (2005) Male microchimerism in women without sons: quantitative assessment and correlation with pregnancy history. (full text). The American Journal of Medicine. 118 (8): 899–906. doi:10.1016/j.amjmed.2005.03.037. PMID 16084184.

