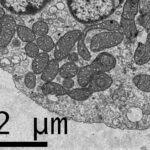
Imagen de microscopio electrónico de barrido del epitelio de la tráquea pulmonar. Hay células ciliadas y no ciliadas en este epitelio. Se aprecia la diferencia de tamaño entre los cilios y las microvellosidades (en la superficie celular no ciliada).
El Síndrome de Bardet-Biedl (BBS por sus siglas en inglés, Bardet-Biedl Syndrome), es una enfermedad rara del grupo de las ciliopatías, trastornos genéticos hereditarios resultantes de defectos en el cilio primario. Pero, ¿qué es el cilio primario?
El cilio primario funciona principalmente como una antena presente en casi todas las células de nuestro cuerpo que capta e integra todas esas señales moleculares extracelulares. Así, los cilios primarios juegan un papel clave en la comunicación entre células y en la coordinación de las diferentes vías de señalización celular.
Como los cilios tienen una distribución casi ubicua en el cuerpo humano, el deterioro de su estructura o función debido a defectos genéticos da como resultado una variedad de condiciones que pueden afectar a múltiples órganos, mientras que la ausencia total de estas estructuras es incompatible con la vida. Es por esto que el BBS presenta sintomatología en la mayoría de los órganos. Los principales rasgos clínicos aparecen representados en la figura 1, desarrollándose la mayoría de ellos en la primera década de vida. Pacientes con cuatro características primarias o tres características primarias y dos secundarias son diagnosticados clínicamente con BBS.
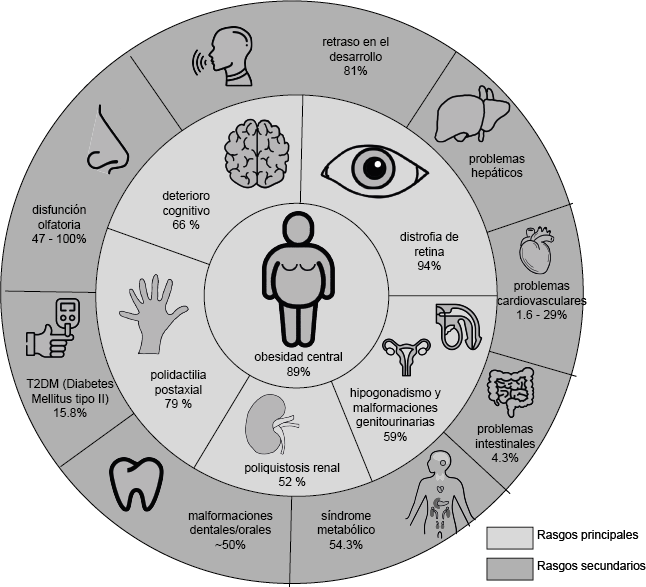
Características principales y secundarias más comunes del fenotipo del síndrome de Bardet-Biedl. Los porcentajes indican la incidencia del rasgo en la población.
Sin embargo, esta enfermedad es más compleja de lo que parece. El BBS es una de las ciliopatías genéticamente más heterogéneas, con 26 genes BBS involucrados hasta la fecha que explican alrededor del 70-80 % de los pacientes diagnosticados clínicamente. En cuanto al patrón de herencia, el BBS se hereda en gran medida como un rasgo autosómico recesivo (deben estar presentes dos copias de un gen anormal, una del padre y otra de la madre, para que se desarrolle la enfermedad o el rasgo). Sin embargo, es posible que miembros de la misma familia, diagnosticados con las mismas alteraciones en los mismos genes BBS, presenten una sintomatología diferente. ¿A qué se puede deber esto? Aún no lo sabemos con certeza, pero este fenómeno sugiere que existen otros mecanismos involucrados en el desarrollo del fenotipo.
Una de las teorías existentes habla de “modulación del fenotipo”. Esta teoría, no solo aplicable a esta enfermedad, sugiere que mutaciones comunes, que pueden estar presentes en la población general sin ningún efecto sobre la salud de quien las porta, pueden agravar la sintomatología de otras enfermedades mediante la interacción con los genes causales de la enfermedad. De esta forma, mutaciones sin ningún efecto sobre la salud de una persona cualquiera puede tener consecuencias graves en un paciente con BBS.
Los genes BBS no tienen la misma carga mutacional. BBS1 es el gen que aparece alterado en mayor número de pacientes (28%), seguido de BBS10 (17%) y los genes BBS2, BBS3 y BBS12 (8%). En la figura 2 aparece la distribución de mutaciones causales a lo largo de genes BBS en la población española, que difiere un poco con la distribución de mutaciones de la población global. En España hay recogidos y descritos en la literatura unos 100 casos de BBS, unos datos relativamente bajos comparado con otras poblaciones europeas, e infinitamente menores comparado con poblaciones que tienden a la consanguinidad (Kuwait, islas Feroe o Terranova).
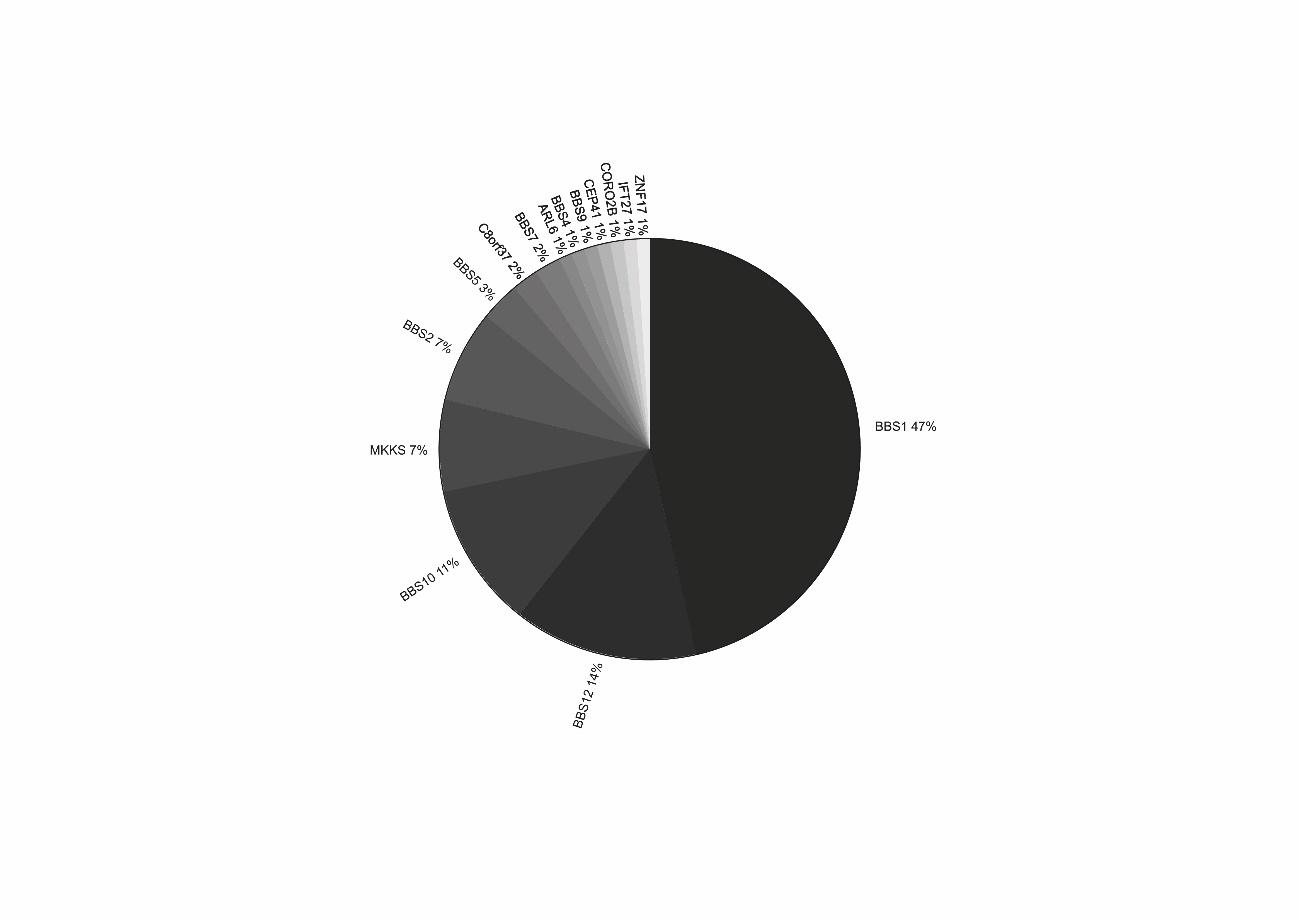
Gráfico que muestra la distribución de los genes causales descritos en la cohorte española. La población española presenta un mayor número de variantes en BBS12 que el resto de las cohortes descritas.
Pero, ¿qué hacen las proteínas codificadas por estos genes y qué relación tienen con el cilio primario? La mayoría de los genes BBS codifican proteínas que se expresan principalmente en el cilio primario. Ocho de las proteínas BBS (BBS1, BBS2, BBS4, BBS5, BBS7, BBS8, BBS9 y BBS18/BBIP10) interactúan físicamente para formar un complejo llamado BBSoma. La función principal de este complejo multiproteico consiste en mediar en el transporte de moléculas dentro y fuera del cilio primario. Además, existen tres proteínas BBS (BBS6, BBS10 y BBS12) que tienen función de chaperona, es decir, son las encargadas del correcto plegamiento y ensamblaje de las 8 proteínas BBS que componen el BBSoma. Las variantes en estas chaperonas se correlacionan con fenotipos más severos.
Por desgracia, actualmente no existe cura para el BBS, y el tratamiento se enfoca en aliviar sus síntomas, en particular en el manejo de la diabetes, la hipertensión y el síndrome metabólico para minimizar el impacto secundario que estas afecciones tienen en los sistemas de órganos vulnerables que ya están afectados por el BBS, en particular los ojos. y riñones.
Sin embargo, aunque se están desarrollando nuevos tratamientos a un ritmo trepidante, incluidas las terapias génicas, ninguno de estos está todavía disponible para su uso en pacientes y se encuentran en diferentes etapas de investigación. Además se están desarrollando otras terapias como la reclasificación de fármacos, medicina personalizada e intervenciones no farmacológicas.